2025年11月,白宫发布了第二轮医保Medicare药价谈判结果,此轮谈判仍然聚焦于Medicare Part D,谈判药品数量从第一轮的10个上升到15个,降幅为38%-85%。根据CMS的测算,如果以2024年的净价来计算,此次降价能带来120亿美元的费用节约,相当于节约了44%的净开支,为个人用户节省6.85亿美元的支出。
与第一轮只节约了60亿美元,即22%的净开支相比,第二轮药价谈判节约的费用占比更高,这主要是受到两个原因影响。第一,第二轮谈判中癌症用药更多,而癌症药品往往是高标价高净价,根据MedPAC的分析,癌症药品的rebate一般只有10%左右。由于《通胀削减法案》(IRA)设置了最低降价幅度,上市9至12年的药品至少降到批发价格的75%,上市12-16年的药品降至65%,上市16年及以上的药品降至40%。也就是降价幅度在25%-60%。因此,仅标价的下降幅度就超过了rebate,净价降幅也就更大了。
第二,此轮谈判中,GLP-1产品司美格鲁肽的加入推动了净开支的下降。根据CMS的公告,2024年,Medicare Part D中有228.2万用户使用司美格鲁肽的三款产品:Ozempic、Rybelsus和Wegovy,总开支为151.6亿美元。根据谈判结果,司美格鲁肽的标价从959美元/月下降到274美元/月,降幅为71%,高剂量的Wegovy价格为385美元/月。
虽然Ozempic的净价在2023年9月为290美元/月,但Wegovy的净价仍处于617美元/月的高价。如果司美格鲁肽的三款产品总开支降幅与此次平均降幅相同,仅这三款药品的开支就相当于削减了66.7亿美元,占到整体削减金额的52.8%。而在2024年的谈判中,排在总花费第一位的是Januvia,2023年在Medicare Part D的花费也只有40.9亿美元。
因此,受到癌症药品的高标价高净价所带来的更大降幅,以及司美格鲁肽的高额花费所带来的费用削减,第二轮谈判节约的药品开支在总金额上和降幅上都会远超第一轮药价谈判。
不过,如果根据2025年已经实施的新报销规则,第二轮药价谈判的成果明显缩减,实际节约的费用缩小到85亿美元,即36%的净开支节约。这主要是因为在IRA的新报销规则下,高价药给到医保的折扣更大,导致医保谈判降价的实际成果没那么大。
比如修美乐(cf)Pen(阿达木单抗),2021年Medicare Part D中该药的每人每年平均花费为56752美元。在老规则下,个人需支付5458美元,商业保险支付10275美元,药企在第三部分支付4582美元,而因为在到达巨灾保障11206美元的起付线以上,还有4万多美元的费用,因此Medicare需要支付巨灾保障的80%部分,也就是36437美元。按比例来看的话,也就是Medicare支付了64%,个人,商业保险,药企分别支付10%,18%和8%。
但在2025年已经实施的新规则下,个人的支付被限制在2000美元,也就是4%的费用。Medicare的支付下降到10053美元,也就是18%。而商业保险和药企的支付金额大幅上升,分别增加231%和132%,商业保险将支付34047美元,药企将支付10651美元,分别占60%和19%。
因此,修美乐在Medicare Part D下给出的折扣从8%上升到19%,增加了11%的折让,这也是药价谈判实际成果缩减的原因。
图表:美国第二轮药价谈判价格
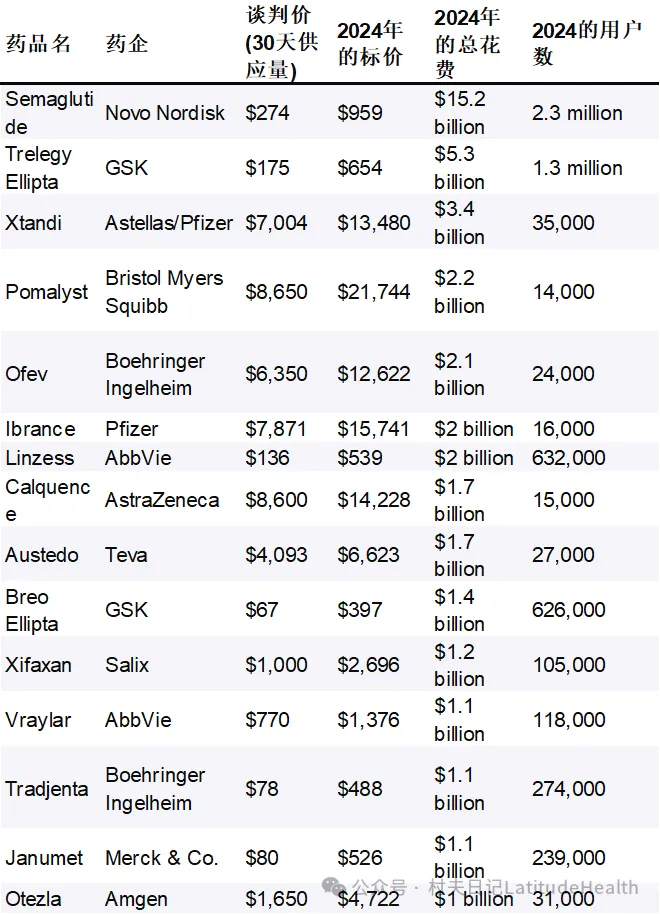
数据来源:CMS
从上述的简要分析来看,连续两轮的美国药价谈判取得了一定的成果,但这些都是在2022年的IRA法案框架下的。而2025年共和党在国会推动的OBBBA(One Big Beautiful Bill Act,减税法案)则在实际上削弱了IRA的效力。
CMS在2025年9月底正式发布了《Medicare Drug Price Negotiation Program Final Guidance for Initial Price Applicability Year 2028 and Manufacturer Effectuation of the Maximum Fair Price in 2026, 2027, and 2028》。指引明确,孤儿药的定义大幅扩大,一种药物可以拥有两个或两个以上的孤儿药认定/批准(designations/approvals),并且无论该药物的销售收入有多少,都永远不会进行医保谈判,而原先只能是有一个适应症的孤儿药才可以豁免。同时,指引允许品牌药的多个适应症中只要有一个孤儿药适应症也可以重新计算谈判时间,计算谈判年限从FDA批准第一个非孤儿药适应症开始计算,而不是从FDA批准第一个适应症开始计算。这将导致一些药物的谈判时间比原先更晚,比如K药和O药的谈判时间将由此推迟一年,从2026年推迟到2027年,降价的实施时间也将从2028年延迟到2029年。
修改孤儿药适应症策略的核心是延迟谈判时间,毕竟单纯的孤儿药是很难成为大单品的,但药王普遍都会有孤儿药的适应症。通过拖延谈判时间,来为药企的营收下降提供缓冲,至于对Medicare的开支带来增加并不是其主要关心的问题。根据CBO地预测,因为孤儿药定义改变将导致Medicare在未来10年多支出至少90亿美元。
根据《Health Affairs》在8月底发布的相关分析,在2026-2030年之间,Medicare年花费超过2亿美元的172个品牌药中,73个品牌药至少有一个孤儿药的适应症,其中28个药符合IRA的标准将被排除在谈判之外,而根据OBBBA,因为有多个孤儿药适应症,15个药品将新获得豁免。另外30个药品是有一个及以上的孤儿药适应症,其中10个药品将有可能推迟谈判时间。
按照第一个适应症来计算,Adcetris已经上市14年,根据OBBBA可以再推迟13.5年,一直到2036年才会进入谈判。Kesimpta/Arezza已经上市15.8年,可以推迟11年,可以到2031年再进入谈判。Opzelura/Jakafi已经上市13.7年,可以推迟10年,到2028年才进入谈判。而K药和O药只推迟了1.1年和0.9年,纳入谈判的时间是2026年9月和11月,这意味着K药和O药要等到2027年才会正式谈判。
美国药企将最大化利用政策来规避价格谈判。主要的策略包括:停止或延缓非孤儿药适应症临床开发,加快孤儿药适应症开发,或者延缓非孤儿药适应症申报的时间。
因此,如果仔细观察美国药价谈判政策,基本的框架仍然基于IRA,而2025年通过的OBBBA则对药价谈判造成了明显的削弱。第二轮药价谈判看似延续并超过了第一轮的降幅,但借助OBBBA,大量高价药避开或推迟了药价谈判,造成了前进与退步并行的局面。
0
推荐




 京公网安备 11010502034662号
京公网安备 11010502034662号 